Sկանդիում, տարրի խորհրդանիշը՝ Sc և ատոմային համարը՝ 21, հեշտությամբ լուծվում է ջրում, կարող է փոխազդել տաք ջրի հետ և հեշտությամբ մգանում է օդում։ Դրա հիմնական վալենտային արժեքը +3 է։ Այն հաճախ խառնվում է գադոլինիումի, էրբիումի և այլ տարրերի հետ՝ ցածր ելքով և կեղևում մոտավորապես 0.0005% պարունակությամբ։ Սկանդիումը հաճախ օգտագործվում է հատուկ ապակի և թեթև բարձր ջերմաստիճանային համաձուլվածքներ պատրաստելու համար։
Ներկայումս աշխարհում սկանդիումի ապացուցված պաշարները կազմում են ընդամենը 2 միլիոն տոննա, որի 90-95%-ը պարունակվում է բոքսիտի, ֆոսֆորիտի և երկաթի, տիտանի հանքաքարերում, իսկ մի փոքր մասը՝ ուրանի, թորիումի, վոլֆրամի և հազվագյուտ հողերի հանքաքարերում, որոնք հիմնականում տարածված են Ռուսաստանում, Չինաստանում, Տաջիկստանում, Մադագասկարում, Նորվեգիայում և այլ երկրներում: Չինաստանը շատ հարուստ է սկանդիումի պաշարներով՝ սկանդիումի հետ կապված հսկայական հանքային պաշարներով: Անավարտ վիճակագրության համաձայն՝ Չինաստանում սկանդիումի պաշարները կազմում են մոտ 600000 տոննա, որոնք պարունակվում են բոքսիտի և ֆոսֆորիտի հանքավայրերում, Հարավային Չինաստանում պորֆիրային և քվարցային երակային վոլֆրամի հանքավայրերում, Հարավային Չինաստանում հազվագյուտ հողերի հանքավայրերում, Ներքին Մոնղոլիայում Բայան Օբոյի հազվագյուտ հողերի երկաթի հանքավայրում և Սիչուանում Պանժիհուայի վանադիումի, տիտանի և մագնետիտի հանքավայրերում:
Սկանդիումի սակավության պատճառով սկանդիումի գինը նույնպես շատ բարձր է, և իր գագաթնակետին սկանդիումի գինը 10 անգամ բարձր էր ոսկու գնից։ Չնայած սկանդիումի գինը նվազել է, այն դեռևս չորս անգամ բարձր է ոսկու գնից։
Պատմության բացահայտում
1869 թվականին Մենդելեևը նկատեց կալցիումի (40) և տիտանի (48) միջև ատոմային զանգվածի տարբերություն և կանխատեսեց, որ այստեղ կա նաև չհայտնաբերված միջանկյալ ատոմային զանգված ունեցող տարր։ Նա կանխատեսեց, որ դրա օքսիդը X ₂ O Å է։ Սկանդիումը հայտնաբերվել է 1879 թվականին Շվեդիայի Ուփսալայի համալսարանի Լարս Ֆրեդերիկ Նիլսոնի կողմից։ Նա այն արդյունահանել է սև հազվագյուտ ոսկու հանքից, որը բարդ հանքաքար է, որը պարունակում է 8 տեսակի մետաղական օքսիդներ։ Նա արդյունահանել էԷրբիում(III) օքսիդսև հազվագյուտ ոսկու հանքաքարից և ստացվել էԻտերբիում(III) օքսիդայս օքսիդից, և կա ավելի թեթև տարրի մեկ այլ օքսիդ, որի սպեկտրը ցույց է տալիս, որ այն անհայտ մետաղ է։ Սա Մենդելեևի կողմից կանխատեսված մետաղն է, որի օքսիդըSc₂O₃Սկանդիում մետաղն ինքնին արտադրվել էՍկանդիումի քլորիդէլեկտրոլիտային հալեցմամբ 1937 թվականին։
Մենդելեև
Էլեկտրոնային կոնֆիգուրացիա
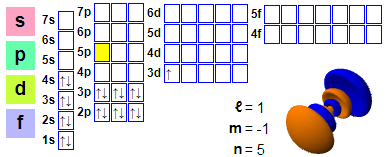
Էլեկտրոնային կոնֆիգուրացիա՝ 1s2 2s2 2p6 3s2 3p6 4s2 3d1
Սկանդիումը փափուկ, արծաթափայլ սպիտակ անցումային մետաղ է, որի հալման ջերմաստիճանը 1541 ℃ է, իսկ եռմանը՝ 2831 ℃։
Հայտնաբերումից հետո զգալի ժամանակահատվածում սկանդիումի օգտագործումը չէր ցուցադրվում դրա արտադրության դժվարության պատճառով: Հազվագյուտ հողային տարրերի բաժանման մեթոդների աճող կատարելագործման հետ մեկտեղ, այժմ գոյություն ունի սկանդիումի միացությունների մաքրման հասուն գործընթաց: Քանի որ սկանդիումը պակաս ալկալային է, քան իտրիումը և լանթանիդը, հիդրօքսիդն ամենաթույլն է, ուստի սկանդիում պարունակող հազվագյուտ հողային տարրերի խառը հանքանյութը կբաժանվի հազվագյուտ հողային տարրից «աստիճանական նստեցման» մեթոդով, երբ սկանդիում(III) հիդրօքսիդը լուծույթի մեջ տեղափոխելուց հետո մշակվում է ամոնիակով: Մյուս մեթոդը սկանդիումի նիտրատի բաժանումն է նիտրատի բևեռային քայքայման միջոցով: Քանի որ սկանդիումի նիտրատն ամենահեշտն է քայքայվում, սկանդիումը կարող է բաժանվել: Բացի այդ, ուղեկցող սկանդիումի համապարփակ վերականգնումը ուրանից, թորիումից, վոլֆրամից, անագից և այլ հանքային հանքավայրերից նույնպես սկանդիումի կարևոր աղբյուր է:
Մաքուր սկանդիումի միացություն ստանալուց հետո այն վերածվում է ScCl3 Å-ի և համատեղ հալվում KCl-ի և LiCl-ի հետ: Հալված ցինկն օգտագործվում է որպես էլեկտրոլիզի կաթոդ, ինչը հանգեցնում է սկանդիումի նստվածքի ցինկի էլեկտրոդի վրա: Այնուհետև ցինկը գոլորշիանում է՝ ստանալով մետաղական սկանդիում: Սա թեթև արծաթափայլ սպիտակ մետաղ է՝ շատ ակտիվ քիմիական հատկություններով, որը կարող է ռեակցիայի մեջ մտնել տաք ջրի հետ՝ առաջացնելով ջրածնային գազ: Այսպիսով, նկարում տեսած մետաղական սկանդիումը փակվում է շշի մեջ և պաշտպանված է արգոն գազով, հակառակ դեպքում սկանդիումը արագ կառաջացնի մուգ դեղին կամ մոխրագույն օքսիդային շերտ՝ կորցնելով իր փայլուն մետաղական փայլը:
Դիմումներ
Լուսավորության արդյունաբերություն
Սկանդիումի կիրառությունները կենտրոնացած են շատ պայծառ ուղղություններով, և չափազանցություն չի լինի այն անվանել Լույսի Որդի։ Սկանդիումի առաջին կախարդական զենքը կոչվում է սկանդիում-նատրիումի լամպ, որը կարող է օգտագործվել հազարավոր տնային տնտեսություններ լույս բերելու համար։ Սա մետաղական հալոգենային էլեկտրական լույս է. լամպը լցված է նատրիումի յոդիդով և սկանդիումի եռիոդիդով, և սկանդիումի և նատրիումի փայլաթիթեղը միաժամանակ ավելացվում են։ Բարձր լարման լիցքաթափման ժամանակ սկանդիումի և նատրիումի իոնները համապատասխանաբար արձակում են իրենց բնորոշ ճառագայթման ալիքի երկարությունների լույս։ Նատրիումի սպեկտրալ գծերը 589.0 և 589.6 նմ են՝ երկու հայտնի դեղին լույսեր, մինչդեռ սկանդիումի սպեկտրալ գծերը 361.3~424.7 նմ են՝ մոտ ուլտրամանուշակագույն և կապույտ լույսի ճառագայթումների շարք։ Քանի որ դրանք լրացնում են միմյանց, ստացված ընդհանուր լույսի գույնը սպիտակ լույս է։ Հենց այն պատճառով, որ սկանդիում-նատրիումային լամպերն ունեն բարձր լուսային արդյունավետության, լավ լույսի գույնի, էներգախնայողության, երկար ծառայության ժամկետի և ուժեղ մառախուղը ցրելու ունակության բնութագրեր, դրանք կարող են լայնորեն օգտագործվել հեռուստատեսային տեսախցիկների, հրապարակների, մարզական վայրերի և ճանապարհների լուսավորության համար և հայտնի են որպես երրորդ սերնդի լույսի աղբյուրներ: Չինաստանում այս տեսակի լամպը աստիճանաբար տարածվում է որպես նոր տեխնոլոգիա, մինչդեռ որոշ զարգացած երկրներում այս տեսակի լամպը լայնորեն օգտագործվել է դեռևս 1980-ականների սկզբին:
Սկանդիումի երկրորդ կախարդական զենքը արևային ֆոտովոլտային մարտկոցներն են, որոնք կարող են հավաքել գետնի վրա ցրված լույսը և այն վերածել էլեկտրաէներգիայի՝ մարդկային հասարակությունը շարժելու համար: Սկանդիումը մետաղական մեկուսիչ, կիսահաղորդչային սիլիցիումային արևային մարտկոցների և արևային մարտկոցների լավագույն արգելապատնեշային մետաղն է:
Դրա երրորդ կախարդական զենքը կոչվում է γ ճառագայթային աղբյուր, այս կախարդական զենքը կարող է պայծառ փայլել ինքնուրույն, բայց այս տեսակի լույսը չի կարող ընկալվել անզեն աչքով, դա բարձր էներգիայի ֆոտոնային հոսք է: Մենք սովորաբար 45Sc-ը արդյունահանում ենք հանքանյութերից, որը սկանդիումի միակ բնական իզոտոպն է: Յուրաքանչյուր 45Sc միջուկ պարունակում է 21 պրոտոն և 24 նեյտրոն: 46Sc-ը, որը արհեստական ռադիոակտիվ իզոտոպ է, կարող է օգտագործվել որպես γ ճառագայթման աղբյուրներ կամ հետագծող ատոմներ, որոնք կարող են նաև օգտագործվել չարորակ ուռուցքների ճառագայթային թերապիայի համար: Կան նաև կիրառություններ, ինչպիսիք են իտրիում-գալիում-սկանդիում-նռնաքարի լազերը,Սկանդիումի ֆտորիդապակե ինֆրակարմիր օպտիկական մանրաթել և սկանդիումով պատված կաթոդային ճառագայթային խողովակ հեռուստացույցի վրա։ Թվում է, թե սկանդիումը ծնվում է պայծառության հետ միասին։
Ալյումինե արդյունաբերություն
Սկանդիումը իր տարրական տեսքով լայնորեն օգտագործվել է ալյումինե համաձուլվածքների հարստացման համար: Քանի դեռ ալյումինին ավելացվում է սկանդիումի մի քանի հազարերորդական մաս, առաջանում է Al3Sc նոր փուլ, որը մետամորֆիզմի դեր է խաղում ալյումինե համաձուլվածքում և զգալիորեն փոխում է համաձուլվածքի կառուցվածքն ու հատկությունները: 0.2%~0.4% Sc ավելացնելը (որը շատ նման է տանը տապակած բանջարեղենին աղ ավելացնելու համամասնությանը, անհրաժեշտ է միայն մի փոքր քանակություն) կարող է բարձրացնել համաձուլվածքի վերաբյուրեղացման ջերմաստիճանը 150-200 ℃-ով և զգալիորեն բարելավել բարձր ջերմաստիճանային ամրությունը, կառուցվածքային կայունությունը, եռակցման կատարողականը և կոռոզիոն դիմադրությունը: Այն նաև կարող է կանխել փխրունության երևույթը, որը հեշտությամբ կարող է առաջանալ բարձր ջերմաստիճաններում երկարատև աշխատանքի ընթացքում: Բարձր ամրության և բարձր կարծրության ալյումինե համաձուլվածքը, նոր բարձր ամրության կոռոզիոն դիմացկուն եռակցվող ալյումինե համաձուլվածքը, նոր բարձր ջերմաստիճանային ալյումինե համաձուլվածքը, բարձր ամրության նեյտրոնային ճառագայթմանը դիմացկուն ալյումինե համաձուլվածքը և այլն ունեն շատ գրավիչ զարգացման հեռանկարներ ավիատիեզերական արդյունաբերության, ավիացիայի, նավերի, միջուկային ռեակտորների, թեթև տրանսպորտային միջոցների և արագընթաց գնացքների ոլորտներում:
Սկանդիումը նաև երկաթի հիանալի մոդիֆիկատոր է, և սկանդիումի փոքր քանակը կարող է զգալիորեն բարելավել թուջի ամրությունն ու կարծրությունը: Բացի այդ, սկանդիումը կարող է օգտագործվել նաև որպես հավելանյութ բարձր ջերմաստիճանի վոլֆրամի և քրոմի համաձուլվածքների համար: Իհարկե, բացի հարսանեկան հագուստ պատրաստելու համար նախատեսված հագուստից, սկանդիումը ունի բարձր հալման կետ, և դրա խտությունը նման է ալյումինին, և այն նաև օգտագործվում է բարձր հալման կետի թեթև համաձուլվածքներում, ինչպիսիք են սկանդիումի տիտանի համաձուլվածքը և սկանդիումի մագնեզիումի համաձուլվածքը: Այնուամենայնիվ, իր բարձր գնի պատճառով այն սովորաբար օգտագործվում է միայն բարձրակարգ արտադրական արդյունաբերություններում, ինչպիսիք են տիեզերանավերն ու հրթիռները:
Կերամիկական նյութ
Սկանդիումը, որպես մեկ նյութ, սովորաբար օգտագործվում է համաձուլվածքներում, և դրա օքսիդները կարևոր դեր են խաղում կերամիկական նյութերում նմանատիպ ձևով: Քառանկյուն ցիրկոնիումային կերամիկական նյութը, որը կարող է օգտագործվել որպես էլեկտրոդային նյութ պինդ օքսիդային վառելիքային բջիջների համար, ունի եզակի հատկություն, որտեղ այս էլեկտրոլիտի հաղորդունակությունը մեծանում է ջերմաստիճանի և շրջակա միջավայրում թթվածնի կոնցենտրացիայի բարձրացման հետ մեկտեղ: Այնուամենայնիվ, այս կերամիկական նյութի բյուրեղային կառուցվածքն ինքնին չի կարող կայուն գոյություն ունենալ և արդյունաբերական արժեք չունի. անհրաժեշտ է ավելացնել որոշ նյութեր, որոնք կարող են ամրացնել այս կառուցվածքը՝ դրա սկզբնական հատկությունները պահպանելու համար: 6~10% սկանդիումի օքսիդի ավելացումը նման է բետոնե կառուցվածքի, այնպես որ ցիրկոնիումը կարող է կայունացվել քառակուսի ցանցի վրա:
Կան նաև ինժեներական կերամիկական նյութեր, ինչպիսիք են բարձր ամրության և բարձր ջերմաստիճանին դիմացկուն սիլիցիումի նիտրիդը, որպես խտացուցիչներ և կայունացուցիչներ։
Որպես խտացուցիչ,Սկանդիումի օքսիդկարող է մանր մասնիկների եզրին առաջացնել Sc2Si2O7 հրակայուն փուլ, այդպիսով նվազեցնելով ինժեներական կերամիկայի բարձր ջերմաստիճանային դեֆորմացիան։ Համեմատած այլ օքսիդների հետ, այն կարող է ավելի լավ բարելավել սիլիցիումի նիտրիդի բարձր ջերմաստիճանային մեխանիկական հատկությունները։
Կատալիտիկ քիմիա
Քիմիական ճարտարագիտության մեջ սկանդիումը հաճախ օգտագործվում է որպես կատալիզատոր, մինչդեռ Sc2O3-ը կարող է օգտագործվել էթանոլի կամ իզոպրոպանոլի ջրազրկման և դեօքսիդացման, քացախաթթվի քայքայման և CO-ից և H2-ից էթիլենի ստացման համար: Sc2O3 պարունակող PtAl կատալիզատորը նաև կարևոր կատալիզատոր է ծանր նավթի հիդրոգենացման մաքրման և զտման գործընթացների համար նավթաքիմիական արդյունաբերության մեջ: Կատալիտիկ կրեկինգի ռեակցիաներում, ինչպիսին է կումոլը, Sc-Y զեոլիտի կատալիզատորի ակտիվությունը 1000 անգամ ավելի բարձր է, քան ալյումինի սիլիկատային կատալիզատորինը. որոշ ավանդական կատալիզատորների համեմատ, սկանդիումի կատալիզատորների զարգացման հեռանկարները շատ պայծառ կլինեն:
Ատոմային էներգիայի արդյունաբերություն
Բարձր ջերմաստիճանի ռեակտորի միջուկային վառելիքի մեջ UO2-ին փոքր քանակությամբ Sc2O3 ավելացնելը կարող է կանխել UO2-ի U3O8-ի փոխակերպման հետևանքով առաջացող ցանցի ձևափոխությունը, ծավալի աճը և ճաքերը։
Վառելիքային բջիջ
Նմանապես, նիկել-ալկալային մարտկոցներին 2.5%-ից մինչև 25% սկանդիում ավելացնելը կերկարացնի դրանց ծառայության ժամկետը։
Գյուղատնտեսական բուծում
Գյուղատնտեսության մեջ սկանդիումի սուլֆատով կարելի է մշակել եգիպտացորենի, ճակնդեղի, ոլոռի, ցորենի և արևածաղկի սերմերը (կոնցենտրացիան սովորաբար 10-3~10-8մոլ/լ է, տարբեր բույսերի դեպքում տարբեր կլինի), և իրական ազդեցությունը բողբոջման խթանման վրա արդեն իսկ ձեռք է բերվել։ 8 ժամ անց արմատների և բողբոջների չոր քաշը համապատասխանաբար աճել է 37%-ով և 78%-ով՝ համեմատած սածիլների հետ, սակայն մեխանիզմը դեռևս ուսումնասիրության փուլում է։
Նիլսենի ատոմային զանգվածի տվյալների նկատմամբ ուշադրությունից մինչև այսօր, սկանդիումը մարդկանց տեսադաշտում է հայտնվել ընդամենը հարյուր կամ քսան տարի, բայց այն գրեթե հարյուր տարի մնացել է անփոփոխ։ Միայն անցյալ դարի վերջին նյութագիտության բուռն զարգացումից հետո այն կենսունակություն բերեց նրան։ Այսօր հազվագյուտ հողային տարրերը, այդ թվում՝ սկանդիումը, դարձել են նյութագիտության տաք աստղեր՝ խաղալով անընդհատ փոփոխվող դերեր հազարավոր համակարգերում, ամեն օր ավելի շատ հարմարավետություն բերելով մեր կյանքին և ստեղծելով տնտեսական արժեք, որն ավելի դժվար է չափել։
Հրապարակման ժամանակը. Հունիս-29-2023